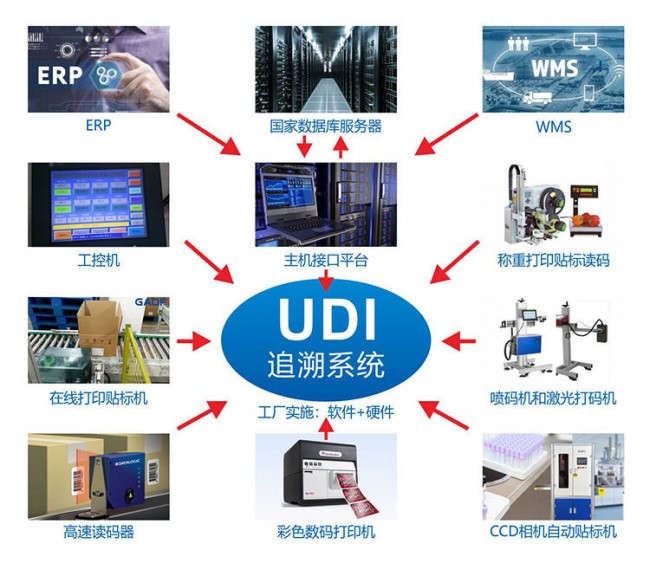
——专访多米诺医疗器械行业发展经理Volker Watzke
根据智研咨询发布的《2017-2022年中国医药市场运行态势及投资战略研究报告》,我国国民医疗需求呈现逐年上升的趋势。医疗产品安全关乎公共健康,偌大的市场如何切实保障医药及器械的安全性,从政府相关机构、医院到医药和器械生产商,肩上的负担都不小。今年7月份的疫苗事件再次将医疗产品的安全性推到舆论的风口浪尖。8月,针对提高医疗器械安全性的举措率先启动,22日,国家市场监督管理总局起草了《医疗器械唯一标识系统规则(征求意见稿)》,旨在利用医疗器械唯一标识,加强医疗器械研制、生产、经营和使用环节的监督和管理,提高监督管理效能,避免类似“疫苗之殇”的事件再次发生。
医疗器械唯一标识,作为改善患者结果的重要工具,欧美国家的成功经验值得我们的借鉴,为了确保医疗器械的安全性和有效性,欧美最早从法律上对“医疗器械medical device”作出明确定义并实行分类管理。以欧盟为例,医疗器械产品在欧盟上市销售前,必须先符合相应的欧盟医疗器械指令。2017年,欧盟颁布新的欧盟医疗器械法规(Medical Devices Regulation, MDR; Regulation (EU) 2017/745)及体外诊断医材法规(In Vitro Diagnostic Medical Devices Regulation, IVDR; Regulation (EU) 2017/746),规定只有带有器械唯一识别码UDI(Unique Device Identification)标识的医疗器械产品,才可以合法进入包含28个成员国的欧盟市场并自由流通。
除了借鉴意义,了解欧盟医疗器械UDI对于我国医疗器械进入国际市场也十分必要,关于欧盟医疗器械UDI的实施,作为众多跨国医疗器械生产商及配线商的首选UDI标识方案供应商,
多米诺公司欧盟医疗器械行业发展经理沃尔克•瓦茨克(Volker Watzke)特别受邀分享其见解。

多米诺公司欧盟医疗器械行业发展经理 沃尔克•瓦茨克(Volker Watzke)
欧盟UDI标识合规期限
过去,欧盟医疗器械的识别需求相对简单,赋码更多集中在生产批号一类信息,不具备可
追溯功能。如果发生医疗事故或者发现器械潜在安全风险需要召回多个产品或特定批次的产品,实施就很艰难。UDI的实施是对这种状况的大变革,实现器械在研发、生产、物流、使用阶段的全程透明性和可追溯性。对于终端使用,沃尔克描述了这样的场景,每个医疗器械上的UDI标识都可使用机器或人眼识别,识别之后,医务人员可以跟踪每种器械的数量,并核实为手术准备的产品是否准确,减少医疗错误的发生、增加患者安全。

关于UDI标识提高器械产品在流通中的透明性和可追溯性,沃尔克还补充,欧盟将建立包含器械认证信息和临床研究、警戒和上市后检测信息的可公开访问的EUDAMED数据库,制造商使用的UDI标识必须在欧洲医疗器械数据库 (EUDAMED)中完成注册。此举确保了在欧洲市场销售的产品都可在EUDAMED得到相关产品,假冒伪劣产品不再具有生存空间。对于未来中国的医疗器械追溯系统具有相当的借鉴意义及可操作性。
而对于在欧盟开展销售业务的中国医疗器械生产企业,沃尔克强调,2020年5月26日,新的MDR法规将在欧盟各成员国强制实行,
多米诺研究显示,UDI标识零基础的企业通常需要12到18个月才能做到UDI合规,企业需要及早规划、布局。除此之外,企业也应注意到不同的医疗器械类别,其UDI赋码的合规是按时间逐步推进。MDR法规中界定的3类器械,Ⅲ类器械指具有重大风险的医疗器械,包括维持生命和拯救生命的器械产品,如心脏起搏器,此类医疗器械生产商将首先面临产品及相关包装上UDI赋码的合规期限,为2021年5月。从2023年5月到2025年5月,UDI赋码合规将在II a/b类和I类医疗器械上推广。同期进行的还有体外诊断器械、A、B、C、D体外诊断器械标签,其截止日期为2027年5月。

如何实施UDI标识赋码?
目前医疗器械生产线上,可用于可变数据赋码的设备非常少。企业不仅需要更新和集成合适的赋码设备,而且还需要及早将数据上载到EUDAMED的识别系统。沃尔克建议企业首先确认产品的类别,产品是否属于极高风险、高风险、中度风险或低风险?所有医疗器械的UDI码注册申请需要在2020年5月26日前完成。
多米诺提供的验证包,将为制造商验证产品并为即将到来的欧盟MDR做准备。
“由于市场上医疗器械产品种类繁多,相应的满足欧盟MDR要求的赋码技术也不在少数。“沃尔克进一步介绍道:“就产品一级最小包装的唯一标识而言,
热发泡喷码机(TIJ)、
热转印打码机(TTO)是不可多得的佳选。如果是在高风险、可重复使用的医疗器械上进行零件的直接赋码,则
激光机(Laser)更合适。对于小型医疗设备制造商,印贴一体技术可以让制造商同时完成标签的赋码和贴标工作,对于多数医疗器械产品,标签可以是铝箔、铝箔、塑料或纸张标签。”
UDI器械标识是提高制造商和有关当局在供应链任一环节追溯相关器械的能力,促使存在安全风险的器材得到即时、高效率的召回的真正有效手段,对于国内医疗器械制造商,应当通过了解UDI实施,率先掌握UDI赋码技术,才能应对国内或将开始逐步实施的医疗器械唯一识别码。
©多米诺标识 版权所有 转载请注明版权来源