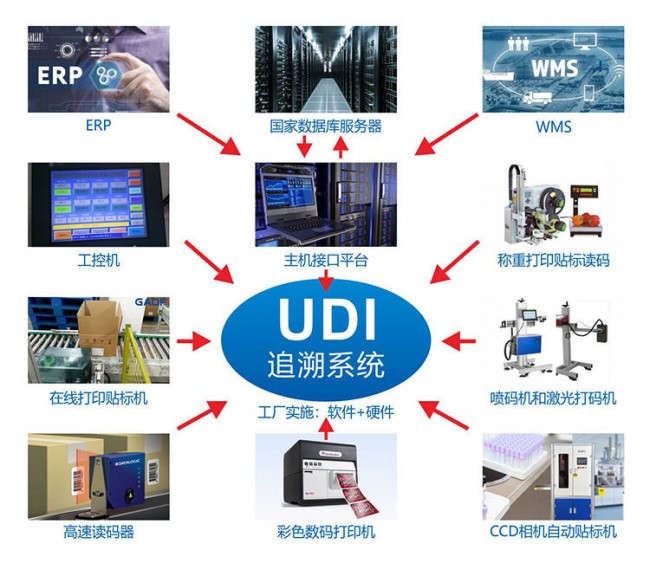
医疗器械产品的分类众多,其中有一类医疗器械是以设备为主体,配备有许多配合治疗使用的关键零部件。在这些医疗器械中,有的零部件仅作为设备的附件配套使用,也有的零部件可以单独使用或销售;有的零部件本身就是医疗器械,也有的零部件本身非医疗器械。种类繁多,令人眼花缭乱。
由于预期用途不同,不同的医疗器械设备可能会出现多种多样的组合情况。面对众多具体使用情况不明的医疗器械关键零部件应该如何完成追溯呢?
关于医疗器械追溯,《医疗器械监督管理条例》中有明确提出:“医疗器械注册人、备案人应当履行建立并执行产品追溯和召回制度的义务。”这就不得不提到实现追溯的基础架构——医疗器械唯一标识(UDI)的实施。“国家根据医疗器械产品类别,分步实施医疗器械唯一标识制度,实现医疗器械可追溯。”因此在完成医疗器械唯一标识的基础上实现追溯是必行之路。
对于追溯一般针对的是医疗器械主体,那么关于医疗器械的关键零部件需要实现追溯吗?又该如何实现追溯呢?
医疗器械的关键零部件是否需要实现追溯需要结合政策法规和实际运用两个方面来看。一方面,需要理清法规对零部件追溯的规定。另一方面也需要结合企业自身的需求和经营企业与医院在使用过程中的需求来判断。

目前没有法规明确且强制要求医疗器械的关键零部件必须实现追溯,因此这里给大家分享一个案例,企业从自身需求出发是如何实现器械零部件追溯的。
A企业的某产品为一款医疗器械设备,该设备配有一部分专属零部件作为附件和该设备主体一起使用,这些零部件有的属于医疗器械,有的不属于医疗器械,在使用时只可配合该设备主体一起使用,不进行单独使用与销售。
考虑到企业成本和器械销售使用方式,应仅对该设备和零部件的整体进行打包赋码,由于零部件不作它用,在追溯该设备的同时也能实现对零部件的追溯,同时也为企业节省了UDI赋码实施的成本。
A企业的某产品由1个医疗器械主体和2个附件组成,这2个零部件本身就属于医疗器械,不仅可以作为附件配合医疗器械使用也可以单独使用。此外,该设备还出口美国,根据美国FDA相关规定,该产品不仅需要在最小销售单元上赋码还需要在使用单元赋码。
因此综合考虑后,应分别为医疗器械主体和每一个零部件赋码的方案,该方案可以同时实现医疗器械主体和零部件的追溯,由于方案选择了最优性价比的方式去完成UDI实施与追溯,企业成本也并未增加多少,却解除了企业的多项合规风险,并为企业完善产品追溯体系打下了良好的基础。