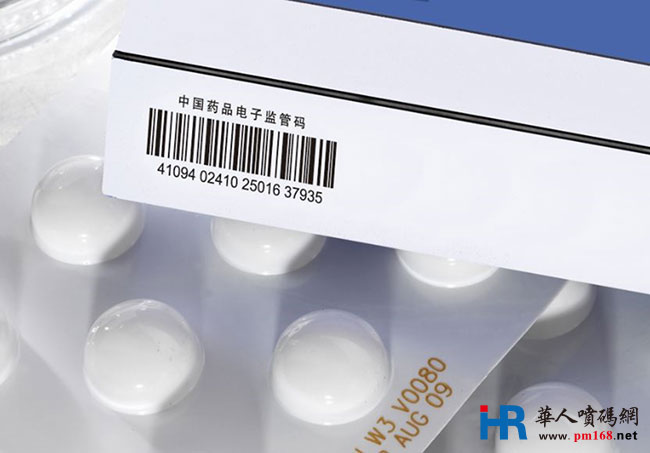
小小一粒药,关系到亿万群众的身体健康和生命安全。我国药品信息化追溯体系建设正稳步推进。

2016年4月28日,国家食药监总局下发了《关于进一步完善食品药品追溯体系的意见(征求意见稿)》。意见指出,食品药品追溯体系是食品药品质量管理体系的重要组成部分。建立食品药品追溯体系是企业的主体责任。
意见还指出,"鼓励生产经营企业运用信息技术建立食品药品追溯体系。鼓励信息技术企业作为第三方,为生产经营企业提供产品追溯专业服务。各级食品药品监管部门不得强制要求食品药品生产经营企业接受指定的专业信息技术企业的追溯服务"。
2017年10月24日质检总局、商务部、中央网信办、国家发展改革委、工信部、公安部、农业部、卫生计生委、安全监管总局、食品药品监管总局等十部门联合印发了《关于开展重要产品追溯标准化工作的指导意见》。
《指导意见》提出,到2020年,要基本建成国家、行业、地方、团体和企业标准相互协同,覆盖全面、重点突出、结构合理的重要产品追溯标准体系。
今年11月,国家药品监督管理局又发布《关于药品信息化追溯体系建设的指导意见》(以下简称《意见》),对药品生产、流通、使用各环节建立覆盖全过程的药品追溯系统提出了完整、系统性的指导意见。

《意见》提出,要加快推进药品信息化追溯体系建设,强化追溯信息互通共享,实现全品种、全过程追溯。明确要求药品上市许可持有人、生产企业、经营企业、使用单位通过信息化手段建立药品追溯系统,及时准确记录、保存药品追溯数据,形成互联互通的药品追溯数据链。药品信息化追溯应实现全品种覆盖,全过程来源可查、去向可追。
《意见》还指出,药品信息化追溯体系建设将分步实施:疫苗、麻醉药品、精神药品、药品类易制毒化学品、血液制品等重点产品应率先建立药品信息化追溯体系;基本药物、医保报销药物等消费者普遍关注的产品尽快建立药品信息化追溯体系;其他药品逐步纳入信息化追溯体系。
业内人士认为,《意见》是对药品信息化追溯体系的顶层设计,体现了建设的总体布局和实施思路,是药品信息化追溯体系建设中重要的里程碑。
政企分工各承其责
“《意见》对各级监管部门、药品生产经营企业、药品使用单位各方在药品追溯体系中承担的责任均给予了明确。”国家药监局药品监管司相关负责人介绍说,《意见》明确,国家药监局的责任是规划确立药品信息化追溯标准体系,明确基本要求,发布追溯体系建设导则,统一药品追溯编码要求、数据及交换标准;建立全国药品信息化追溯协同服务平台,不断完善药品追溯数据交换、共享机制。

药品上市许可持有人、生产企业、经营企业、使用单位是药品质量安全的责任主体,负有追溯义务。《意见》明确,药品上市许可持有人和生产企业承担药品追溯系统建设的主要责任,履行药品信息化追溯管理责任,按照统一药品追溯编码要求,对产品各级销售包装单元赋以唯一追溯标识,以实现信息化追溯。药品经营、使用单位则要积极配合持有人,建成完整的药品追溯系统,履行各自追溯责任。
一物一码统一标准
《意见》提出“一物一码,物码同追”的指导思想,即每个药品的最小包装单元上都具有唯一性的身份编码,通过编码将企业、流通环节、消费者联通起来。早在2005年,我国即开始推行药品电子监管码,不少企业已按照“一物一码”的标准建立了药品追溯体系。中国作为全球制药大国、ICH成员、药品国际供应链的参与者,“一物一码”体现了追求高标准追溯体系的建设目标。

据介绍,药品追溯系统中将实现多种编码并存,既兼容原电子监管码,也兼容国际常用的GS1编码,由企业自主选择、自建追溯体系,企业在原电子监管工作中的投入仍可继续发挥作用。
惠及患者拓展价值
专家指出,《意见》还体现了社会各方广泛参与、拓展数据价值的思路。
如《意见》提出监管部门要创新工作机制,开展形式多样的示范创建活动。要加强舆论正面宣传,培养公众增强药品信息化追溯意识。
各级药品监管部门基于药品信息化追溯体系构建大数据监管系统,有助于创新药品安全监管手段,探索实施药品全过程信息化、智能化监管,完善风险预警机制。充分发挥药品追溯数据在问题产品召回及应急处置中的作用,进一步挖掘药品追溯数据在监督检查、产品抽检和日常监管中的应用价值。